今天為大家分享一篇近期發(fā)表在臨床腫瘤學(xué)TOP期刊《Clinical Cancer Research》的研究,題目為 “68Ga-NK224 PET/CT for Non-Invasive Evaluation of PD-L1 Expression and
Inter-Tumor Heterogeneity: A Translational Exploratory Study”。在這篇文章中,研究團(tuán)隊(duì)開發(fā)了一種靶向PD-L1的新型環(huán)肽放射性探針68Ga-NK224,展示了其在非小細(xì)胞肺癌(NSCLC)患者中無創(chuàng)評(píng)估PD-L1表達(dá)并揭示瘤間異質(zhì)性方面的臨床轉(zhuǎn)化潛力。本文的通訊作者是廈門大學(xué)附屬第一醫(yī)院的陳皓鋆教授、林勤教授、鐘山教授,第一作者是廈門大學(xué)附屬第一醫(yī)院趙亮主治醫(yī)師、逄一臻博士和丁毅副主任醫(yī)師。
研究背景介紹
免疫檢查點(diǎn)抑制劑(ICB)特別是針對(duì)PD-1/PD-L1通路的治療策略,已顯著改善多種惡性腫瘤患者的生存結(jié)局。PD-L1表達(dá)是目前指導(dǎo)免疫治療的重要生物標(biāo)志物,但傳統(tǒng)組織活檢存在取樣局限,無法準(zhǔn)確反映全身病灶及其動(dòng)態(tài)變化,亟需一種無創(chuàng)、可重復(fù)、全身性的檢測(cè)手段。
靶向PD-1及其配體PD-L1的免疫檢查點(diǎn)抑制劑(ICB)已成為包括非小細(xì)胞肺癌(NSCLC)在內(nèi)的多種惡性腫瘤治療的重要基石之一。然而,如何精準(zhǔn)篩選最可能獲益的患者仍是臨床面臨的一大挑戰(zhàn)。目前,PD-L1表達(dá)、腫瘤突變負(fù)荷(TMB)、微衛(wèi)星不穩(wěn)定性(MSI)等生物標(biāo)志物被用于指導(dǎo)免疫治療,其中PD-L1腫瘤比例評(píng)分(TPS)是NSCLC中常用的生物標(biāo)志物。盡管如此,PD-L1的表達(dá)水平與療效并非完全一致,部分高表達(dá)患者療效不佳,而低表達(dá)甚至陰性者亦可受益,提示傳統(tǒng)組織活檢存在取樣局限,無法準(zhǔn)確反映全身病灶及其動(dòng)態(tài)變化,亟需一種無創(chuàng)、可重復(fù)、全身性的檢測(cè)手段。
核醫(yī)學(xué)分子影像,特別是PET技術(shù),具備非侵入、全身覆蓋和定量評(píng)估的特點(diǎn),已成為靶向表達(dá)可視化的有力工具。盡管已有抗PD-L1抗體放射探針用于PET成像研究,但其成像時(shí)間長(zhǎng)、成本高、免疫原性強(qiáng)等問題限制了臨床推廣。相比之下,小分子肽類探針具備快速清除、良好組織穿透性和高對(duì)比成像等優(yōu)勢(shì),成為更具前景的替代選擇。
本研究中,作者團(tuán)隊(duì)開發(fā)了一種特異性靶向PD-L1的環(huán)肽類分子探針NK224,使用NOTA螯合劑實(shí)現(xiàn)與68Ga/18F的高效標(biāo)記,具有良好的體內(nèi)分布性質(zhì)及PD-L1靶向親和力。在臨床前系統(tǒng)評(píng)估的基礎(chǔ)上,研究團(tuán)隊(duì)進(jìn)一步完成了68Ga-NK224在NSCLC患者中的臨床轉(zhuǎn)化研究,探索其在PD-L1表達(dá)可視化、腫瘤異質(zhì)性評(píng)估以及免疫治療靶點(diǎn)占用監(jiān)測(cè)中的應(yīng)用潛力。
研究結(jié)果
68Ga/18F-NK224的體外性能評(píng)價(jià)
NK224是一種14個(gè)氨基酸的環(huán)狀多肽,其序列為環(huán)- (Ac-Tyr-NMeAla-Asn-Pro-His-Glu-Hyp-Trp-Ser-Trp- NMeNle-NMeNle-Lys-Cys)-Gly-NH2,將NOTA作為螯合劑連接NK224,合成可用于18F和68Ga標(biāo)記的靶向探針NK224(圖1A)。放射性標(biāo)記后的68Ga-NK224與18F-NK224比活度均達(dá)30 GBq/μmol以上,放射化學(xué)純度≥99%,在PBS和FBS中2小時(shí)內(nèi)保持高度穩(wěn)定(圖1B-C)。
在細(xì)胞水平,68Ga-NK224對(duì)PD-L1具有良好的結(jié)合親和力(IC50 = 2.45 nM)(圖1D)。在不同PD-L1表達(dá)水平的細(xì)胞系中(U87-MG > C666-1 > A549),探針攝取量與PD-L1表達(dá)呈高度正相關(guān)(圖1E-G)。阻斷實(shí)驗(yàn)顯示,過量未標(biāo)記NK224或PD-L1商品化抗體可使探針攝取降低90%以上,證實(shí)其特異性(圖1E)。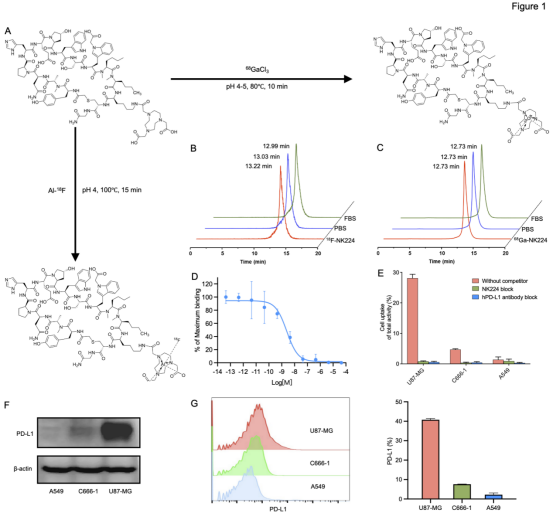
圖1. 68Ga-NK224和18F -NK224的體外評(píng)價(jià)。(A) NK224的化學(xué)結(jié)構(gòu)及其放射性標(biāo)記示意圖。(B-C) 68Ga-NK224和18F-NK224在PBS和FBS中的穩(wěn)定性分析。(D) NK224與PD-L1的結(jié)合親和力評(píng)估。(E) 68Ga-NK224在A549、C666-1和U87-MG細(xì)胞中的攝取與阻斷實(shí)驗(yàn)。(F-G) A549、C666-1和U87-MG細(xì)胞中PD-L1表達(dá)水平的western blot和流式細(xì)胞術(shù)檢測(cè)結(jié)果。
68Ga-NK224和18F-NK224的體內(nèi)性能評(píng)價(jià)
在高表達(dá)PD-L1的U87-MG荷瘤小鼠模型中,68Ga-NK224顯示了良好的體內(nèi)分布及靶向特異性。小動(dòng)物PET顯像顯示,注射后1小時(shí)和2小時(shí),68Ga-NK224在腫瘤內(nèi)的攝取與對(duì)照探針68Ga-WL12(已進(jìn)入臨床試驗(yàn)的PD-L1探針)相當(dāng),但在肝、腎、肺等正常器官的背景攝取顯著更低,從而獲得了更高的腫瘤/背景比(圖2A)。當(dāng)同時(shí)注射過量未標(biāo)記的NK224或hPD-L1抗體后,腫瘤攝取顯著降低,進(jìn)一步驗(yàn)證了探針的PD-L1靶向特異性。離體組織生物分布結(jié)果與PET成像高度一致(圖2B)。在相同動(dòng)物模型中,使用18F標(biāo)記的NK224也獲得了與68Ga-NK224一致的腫瘤顯像效果,在1-2小時(shí)內(nèi)均可實(shí)現(xiàn)清晰成像,具備良好的腫瘤/背景比(圖2C),展現(xiàn)跨放射性核素平臺(tái)的一致性。為了進(jìn)一步驗(yàn)證探針識(shí)別不同PD-L1表達(dá)水平的能力,研究使用了U87-MG(高表達(dá))、C666-1(中表達(dá))和A549(低表達(dá))三種異種移植瘤模型。結(jié)果顯示,68Ga-NK224的腫瘤攝取量與PD-L1表達(dá)量高度相關(guān),呈現(xiàn)U87-MG > C666-1 > A549的趨勢(shì)(圖2D),與相應(yīng)腫瘤組織的PD-L1免疫組化染色結(jié)果相符(圖2E)。
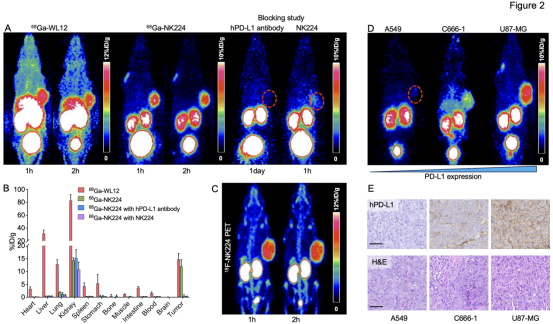
圖2. 68Ga-NK224和18F-NK224的體內(nèi)評(píng)價(jià)。(A) U87-MG腫瘤模型中使用68Ga-WL12和68Ga-NK224的代表性PET顯像圖像,以及68Ga-NK224的阻斷實(shí)驗(yàn)圖像;(B) U87-MG腫瘤模型中68Ga-WL12與68Ga-NK224的組織分布定量結(jié)果,包括68Ga-NK224的阻斷實(shí)驗(yàn)數(shù)據(jù);(C) U87-MG腫瘤模型中18F-NK224的代表性PET顯像圖像;(D) A549、C666-1和U87-MG荷瘤小鼠在注射后1小時(shí)的代表性PET圖像,顯示PD-L1特異性的腫瘤攝取情況;(E) 對(duì)應(yīng)腫瘤組織的PD-L1免疫組化染色及H&E染色圖像。
68Ga-NK224具有良好的體內(nèi)分布性質(zhì)和臨床安全性
3名健康志愿者的劑量學(xué)分析顯示,使用OLINDA軟件計(jì)算的有效劑量為2.06E-02 mSv/MBq,符合核醫(yī)學(xué)放射性探針的輻射安全標(biāo)準(zhǔn)。放射性示蹤劑體內(nèi)主要分布于脾臟和肝臟,未見其他臟器的異常濃聚(圖3A-B)。2023年5月至2024年11月,團(tuán)隊(duì)開展了一項(xiàng)前瞻性臨床轉(zhuǎn)化研究,共納入37例肺癌患者接受68Ga-NK224 PET/CT掃描,其中31例具備PD-L1免疫組化染色結(jié)果并納入分析。無論是健康志愿者還是肺癌患者,注射后 4 小時(shí)內(nèi)所有受試者均無不良反應(yīng),表現(xiàn)出良好臨床安全性。
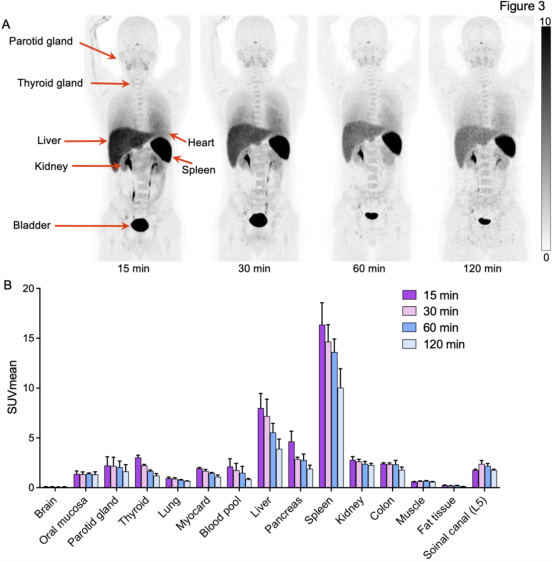
圖3. 68Ga-NK224在3位健康志愿者體內(nèi)的分布情況。(A)注射后15、30、60和120分鐘的代表性PET成像,顯示示蹤劑在正常器官中的分布情況。(B)主要器官(包括肝臟、脾臟、肺部和腎臟)在注射后15、30、60和120分鐘的SUVmean半定量分析。
NSCLC患者PD-L1表達(dá)與68Ga-NK224攝取高度相關(guān),而與18F-FDG攝取無關(guān)
本研究納入的31例肺癌患者中28例為初治患者接受PET/CT初始分期,3例用于評(píng)估腫瘤復(fù)發(fā)轉(zhuǎn)移。26例患者獲取了肺部腫瘤活檢標(biāo)本,6例獲取了肺外轉(zhuǎn)移灶標(biāo)本(1例同時(shí)獲取原發(fā)灶和骨轉(zhuǎn)移灶標(biāo)本)。根據(jù)PD-L1表達(dá)水平,11例為陰性表達(dá)(<1%),14例中表達(dá)(1-49%),7例高表達(dá)(≥50%)。PD-L1陰性、中、高表達(dá)組68Ga-NK224的SUVmax中位數(shù)(四分位距)分別為2.6(2.0-3.3)、4.3(3.7-4.9)和7.8(7.3-11.8)。18F-FDG攝取與PD-L1表達(dá)無相關(guān)性(圖4A),而68Ga-NK224攝取與PD-L1表達(dá)呈顯著正相關(guān)(圖4B,p<0.001)。圖4C展示了不同PD-L1表達(dá)水平患者的代表性68Ga-NK224 PET/CT圖像及免疫組化染色結(jié)果。
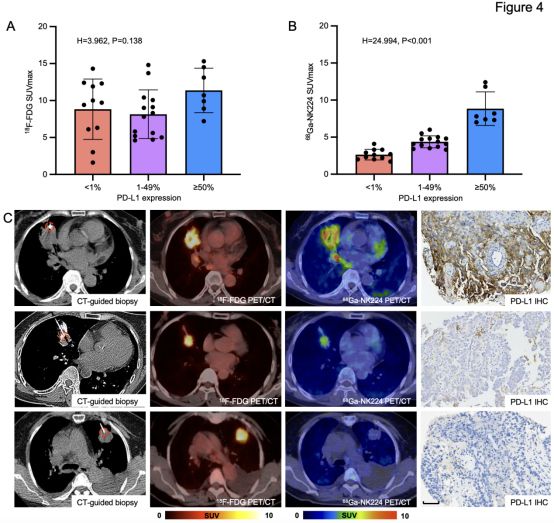
圖4. 68Ga-NK224腫瘤攝取與PD-L1表達(dá)水平的相關(guān)性分析。(A-B)Kruskal-Wallis檢驗(yàn)結(jié)果顯示:18F-FDG SUVmax與PD-L1表達(dá)無顯著相關(guān)性(P=0.138),而68Ga-NK224 SUVmax與PD-L1表達(dá)呈顯著相關(guān)(H=24.994,P<0.001)。(C)不同PD-L1表達(dá)水平患者的18F-FDG與68Ga-NK224 PET/CT圖像及對(duì)應(yīng)免疫組化染色標(biāo)本(紅圈標(biāo)示CT引導(dǎo)下活檢部位)的代表性病例。上排:18F-FDG SUVmax 15.3,68Ga-NK224 SUVmax 8.2,PD-L1 TPS 80%;中排:18F-FDG SUVmax 10.1,68Ga-NK224 SUVmax 4.8,PD-L1 TPS 2%;下排:18F-FDG SUVmax 10.4,68Ga-NK224 SUVmax 2.2,PD-L1 TPS <1%。比例尺:50μm。
31例患者共檢出31個(gè)肺部腫瘤和215個(gè)轉(zhuǎn)移灶。肺部腫瘤與轉(zhuǎn)移灶的68Ga-NK224 SUVmax中位數(shù)均為4.1(四分位距分別為3.3-4.9和2.6-5.8),組間無顯著差異(p=0.709)。Spearman相關(guān)性分析顯示246個(gè)腫瘤病灶的68Ga-NK224攝取與病灶大小無顯著關(guān)聯(lián)(p=0.187),提示其攝取更可能反映靶點(diǎn)表達(dá)而非腫瘤大小。為評(píng)估68Ga-NK224 PET/CT可視化腫瘤PD-L1表達(dá)異質(zhì)性的能力,研究者分析了同一患者不同病灶的攝取差異。圖5A展示典型病例:肺部原發(fā)灶(PD-L1低表達(dá),SUVmax 5.0)與骨轉(zhuǎn)移灶(PD-L1高表達(dá),SUVmax 11.8)的68Ga-NK224攝取差異顯著,而二者18F-FDG攝取相近(原發(fā)灶SUVmax 7.8,骨轉(zhuǎn)移灶8.6)。31例患者中24例存在多發(fā)性轉(zhuǎn)移灶,這些患者病灶間68Ga-NK224 SUVmax的中位變異系數(shù)(CV)達(dá)27.5%(范圍5.7%-53.2%)。為進(jìn)一步評(píng)估68Ga-NK224 PET/CT在識(shí)別患者體內(nèi)PD-L1表達(dá)異質(zhì)性方面的能力,通過數(shù)據(jù)可視化展示了每位患者不同病灶之間的探針攝取差異(圖5B)。

圖5. 68Ga-NK224 PET/CT可視化患者內(nèi)PD-L1表達(dá)異質(zhì)性。(A)轉(zhuǎn)移性NSCLC患者的代表性PET/CT圖像:18F-FDG在原發(fā)灶(紅色箭頭,SUVmax 7.8)與骨轉(zhuǎn)移灶(藍(lán)色箭頭,SUVmax 8.6)攝取相似;68Ga-NK224在兩者攝取差異顯著(原發(fā)灶SUVmax 5.0,骨轉(zhuǎn)移灶SUVmax 11.8);隨后CT引導(dǎo)活檢及免疫組化證實(shí):肺病灶PD-L1低表達(dá),骨轉(zhuǎn)移灶PD-L1高表達(dá);(B)24例患者病灶68Ga-NK224攝取(SUVmax)全景展示:包含24個(gè)原發(fā)灶和215個(gè)轉(zhuǎn)移灶,圖示呈現(xiàn)SUVmax值、腫瘤大小、活檢部位等多維度參數(shù)上的差異。
連續(xù)68Ga-NK224 PET/CT監(jiān)測(cè)PD-L1靶點(diǎn)可及性,指導(dǎo)PD-L1免疫治療給藥頻率
為評(píng)估抗PD-L1抗體對(duì)腫瘤PD-L1靶點(diǎn)的結(jié)合情況,本研究對(duì)接受PD-L1免疫治療的NSCLC患者進(jìn)行了連續(xù)的68Ga-NK224 PET/CT掃描,時(shí)間節(jié)點(diǎn)包括治療前基線及治療后1、7、21天。如圖6所示,基線期NSCLC原發(fā)灶的68Ga-NK224攝取顯著,表明腫瘤對(duì)該顯像劑的親和力較強(qiáng)。經(jīng)過抗PD-L1免疫治療后,患者在治療后1天和7天的腫瘤68Ga-NK224攝取明顯降低,提示治療初期藥物對(duì)PD-L1靶點(diǎn)的有效結(jié)合與抑制作用。然而,在治療后21天時(shí),病灶對(duì)68Ga-NK224的攝取出現(xiàn)輕度升高,這表明抗PD-L1抗體在超過21天的時(shí)間內(nèi)仍能有效占據(jù)PD-L1靶點(diǎn)。此外,研究還發(fā)現(xiàn),接受抗PD-L1免疫治療后,肝臟、脾臟和骨髓的68Ga-NK224攝取顯著降低,而正常肺組織的顯像劑攝取變化較小。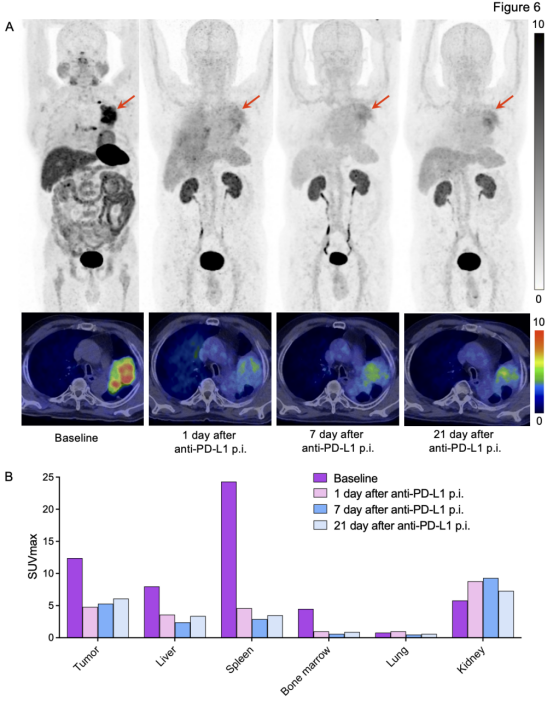
圖6. PD-L1抗體治療前后連續(xù)68Ga-NK224 PET/CT掃描評(píng)估。(A)NSCLC患者治療前和PD-L1抗體給藥后第1、7和21天的68Ga-NK224 PET/CT圖像;(B)柱狀圖描繪了PD-L1抗體治療前后腫瘤、肝臟、脾臟、骨髓、肺和腎臟等主要器官的SUVmax變化。
最后,研究團(tuán)隊(duì)探討了連續(xù)68Ga-NK224 PET顯像動(dòng)態(tài)監(jiān)測(cè)免疫治療期間PD-L1的靶點(diǎn)狀態(tài),進(jìn)而評(píng)估腫瘤病灶中PD-L1抗體對(duì)相應(yīng)靶點(diǎn)的占用情況,從而為PD-L1免疫治療的頻率提供指導(dǎo)(見圖7A-B)。在U87-MG移植瘤小鼠模型中,基線期腫瘤對(duì)68Ga-NK224表現(xiàn)出高度攝取(見圖7C)。在接受PD-L1抗體(10 mg/kg)治療后的第1和第3天,腫瘤攝取持續(xù)下降,而在治療后的第5和第7天,腫瘤攝取略有回升(第3天為0.6±0.2% ID/g,第7天為1.7±0.2% ID/g,見圖7D),這證實(shí)了PD-L1抗體在腫瘤病灶中至少持續(xù)了7天的靶點(diǎn)占用。
為了探索PD-L1分子影像引導(dǎo)的靶點(diǎn)監(jiān)測(cè)在免疫治療優(yōu)化中的價(jià)值,研究團(tuán)隊(duì)比較了兩種給藥方案:一種是基于68Ga-NK224 PET指導(dǎo)的每周一次給藥方案,另一種是傳統(tǒng)的每周三次給藥方案。在hu-CD34+人源化免疫系統(tǒng)小鼠的U87-MG異種移植瘤模型中,對(duì)照組腫瘤快速進(jìn)展,而兩種hPD-L1抗體方案均有效抑制了腫瘤生長(zhǎng)。值得注意的是,68Ga-NK224 PET指導(dǎo)下的低頻給藥組的療效并未遜色于傳統(tǒng)治療方案(見圖7E-F)。這表明,連續(xù)的68Ga-NK224 PET可在免疫治療期間動(dòng)態(tài)監(jiān)測(cè)病灶中的PD-L1表達(dá),有望作為指導(dǎo)PD-L1抗體治療頻率和劑量調(diào)整的精準(zhǔn)工具,具有實(shí)現(xiàn)個(gè)體化治療策略優(yōu)化的潛力。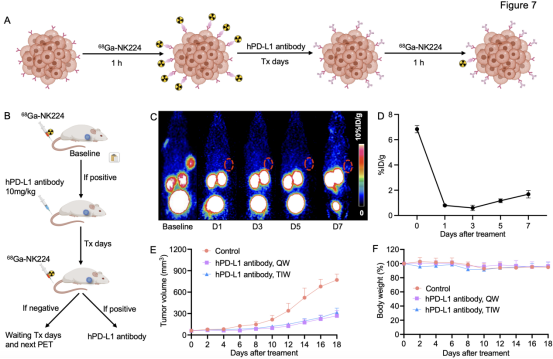
圖7. 利用68Ga-NK224 PET動(dòng)態(tài)監(jiān)測(cè)hPD-L1靶點(diǎn)占用率,指導(dǎo)hPD-L1抗體給藥頻率。(A)使用hPD-L1抗體治療前后,68Ga-NK224 PET顯像評(píng)估可利用的PD-L1靶點(diǎn)的示意圖;(B)實(shí)驗(yàn)設(shè)計(jì)說明了68Ga-NK224 PET對(duì)hPD-L1靶點(diǎn)變化的動(dòng)態(tài)可視化,為優(yōu)化給藥間隔提供了見解;(C-D)PET成像結(jié)果和定量分析68Ga-NK224在基線和hPD-L1抗體給藥后第1,3,5和7天的腫瘤攝取。紅色圓圈表示腫瘤區(qū)域。(E-F)給藥頻率為每周1次(QW)組、常規(guī)頻率為每周3次(TIW)組和生理鹽水對(duì)照組腫瘤生長(zhǎng)曲線和體重變化的比較。
結(jié)論
基于NK224的新型PD-L1靶向多肽,兼具優(yōu)良的腫瘤靶本底比及體內(nèi)分布性質(zhì),能夠準(zhǔn)確評(píng)估全身腫瘤病灶中PD-L1的表達(dá)水平,并能清晰可視化其PD-L1空間異質(zhì)性。此外,該探針還能動(dòng)態(tài)監(jiān)測(cè)免疫治療期間病灶中的PD-L1靶點(diǎn)狀態(tài),為免疫治療的個(gè)體化給藥頻率優(yōu)化提供了全新的影像學(xué)工具與策略支持。這一研究為腫瘤免疫治療的精準(zhǔn)化發(fā)展開辟了新的方向。
原文鏈接:https://doi.org/10.1158/1078-0432.CCR-25-0160
通訊作者簡(jiǎn)介

陳皓鋆,廈門大學(xué)附屬第一醫(yī)院核醫(yī)學(xué)科&閩南PET中心副主任,科研處副主任,臨床醫(yī)學(xué)研究院副院長(zhǎng)。教授,博士生導(dǎo)師,國(guó)家優(yōu)秀青年科學(xué)基金獲得者。研究方向?yàn)楹酸t(yī)學(xué)顯像及治療的臨床轉(zhuǎn)化。擔(dān)任核醫(yī)學(xué)頂刊J Nucl Med編委、 Eur J Nucl Med Mol Imaging編委、《中華核醫(yī)學(xué)與分子影像雜志》編委;主持國(guó)家自然科學(xué)基金3項(xiàng),并主持福建省杰出青年科學(xué)基金、福建省衛(wèi)健委重大項(xiàng)目。入選中國(guó)研究型醫(yī)院評(píng)價(jià)遴選“研究型人才”、福建省衛(wèi)健委“高層次領(lǐng)軍人才”;榮獲中華醫(yī)學(xué)會(huì)核醫(yī)學(xué)分會(huì)“希望之星”、北美核醫(yī)學(xué)與分子影像學(xué)會(huì)“青年科學(xué)家”獎(jiǎng)(SNMMI Ones to Watch,全球30名)。

林勤,主任醫(yī)師,廈門大學(xué)教授,博士生導(dǎo)師,廈門大學(xué)附屬第一醫(yī)院黨委副書記。現(xiàn)任中華醫(yī)學(xué)會(huì)放射腫瘤治療學(xué)分會(huì)委員,福建省醫(yī)學(xué)會(huì)放射腫瘤治療學(xué)分會(huì)副主任委員,福建省抗癌協(xié)會(huì)鼻咽癌專業(yè)委員會(huì)副主任委員,廈門市醫(yī)學(xué)會(huì)腫瘤放療分會(huì)主任委員。任《中華放射醫(yī)學(xué)與防護(hù)雜志》等多種期刊編委。美國(guó)得克薩斯大學(xué)M.D. Anderson 癌癥中心訪問學(xué)者,美國(guó)Duke University訪問學(xué)者。主持或已主持國(guó)家自然科學(xué)基金、福建省衛(wèi)生廳、廈門市科技局及全國(guó)多中心前瞻性臨床研究廈門分中心等多項(xiàng)課題。研究?jī)?nèi)容多次在美國(guó)國(guó)際放射腫瘤學(xué)年會(huì)上壁報(bào)交流。近五年以通訊作者在Clin Cancer Res、J Nucl Med、Signal Transduction and Targeted Therapy、 Eur J Nucl Med Mol Imaging、Radiotherapy & Oncology、Theranostics、中華核醫(yī)學(xué)與分子影像雜志等期刊發(fā)表研究論著20余篇。主要研究方向:分子影像引導(dǎo)下的鼻咽癌、肺癌、肝癌等領(lǐng)域的腫瘤精確放療以及SBRT(立體定向低分割放射治療)。

鐘山,病理科副主任(主持工作),主任醫(yī)師。從事病理診斷工作20多年。擅長(zhǎng)腫瘤病理診斷,精于術(shù)中冰凍、免疫組化及分子病理診斷。有豐富的臨床教學(xué)經(jīng)驗(yàn),系國(guó)家級(jí)住院醫(yī)師規(guī)范化培訓(xùn)基地主任。發(fā)表多篇學(xué)術(shù)論文,參編多項(xiàng)行業(yè)指南。兼任中華醫(yī)學(xué)會(huì)病理分會(huì)學(xué)組委員、廈門市病理質(zhì)控中心主任委員、廈門市醫(yī)學(xué)會(huì)病理學(xué)分會(huì)主任委員。
第一作者簡(jiǎn)介

趙亮,廈門大學(xué)附屬第一醫(yī)院核醫(yī)學(xué)科&閩南PET中心主治醫(yī)師。以第一/通訊作者在J Clin Invest、Clin Cancer Res(2篇)、Radiology、J Nucl Med(6篇)、Eur J Nucl Med Mol Imaging(7篇)、Signal Transduction and Targeted Therapy、Theranostics、JITC等國(guó)際權(quán)威期刊發(fā)表論著31篇(5篇入選ESI高被引論文)、個(gè)案報(bào)道8篇,H影響因子25,累計(jì)被引超過2600次。連續(xù)入選2022、2023全球“前2%頂尖科學(xué)家”榜單(world’s top 2% scientists),獲得2023、2024、2025年北美核醫(yī)學(xué)與分子影像學(xué)會(huì)Alavi-Mandell獎(jiǎng),2024年北美核醫(yī)學(xué)與分子影像年會(huì)國(guó)際最佳摘要和旅行獎(jiǎng),并以主要完成人獲廈門市科技進(jìn)步二等獎(jiǎng)、福建省科技進(jìn)步三等獎(jiǎng)、福建省抗癌協(xié)會(huì)科技進(jìn)步獎(jiǎng)二等獎(jiǎng)。

逄一臻,廈門大學(xué)2021級(jí)腫瘤學(xué)博士研究生,導(dǎo)師為廈門大學(xué)附屬第一醫(yī)院林勤教授和陳皓鋆教授,碩博在讀期間以第一作者/共同第一作者在J Clin Invest、Clin Cancer Res、Radiology、J Nucl Med、Eur J Nucl Med Mol Imaging、Signal Transduction and Targeted Therapy、JITC等國(guó)際權(quán)威期刊發(fā)表研究論文多篇。多次碩士及博士研究生國(guó)家獎(jiǎng)學(xué)金,獲得2021歐洲核醫(yī)學(xué)會(huì)(EANM)“年度最佳論文獎(jiǎng)”、2024年北美核醫(yī)學(xué)協(xié)會(huì)Alavi-Mandell獎(jiǎng),以共同完成人身份獲廈門市科技進(jìn)步二等獎(jiǎng)、福建省抗癌協(xié)會(huì)科技進(jìn)步獎(jiǎng)二等獎(jiǎng)。

丁毅,副主任醫(yī)師,畢業(yè)于福建醫(yī)科大學(xué)病理學(xué)專業(yè),從事病理診斷近20年,曾于北京友誼醫(yī)院病理科進(jìn)行淋巴造血系統(tǒng)亞專科進(jìn)修,師從國(guó)內(nèi)著名淋巴瘤專家周小鴿教授。福建省醫(yī)學(xué)會(huì)消化病學(xué)分會(huì)消化病理學(xué)組委員,福建省醫(yī)師協(xié)會(huì)病理科醫(yī)師分會(huì)胸肺疾病專業(yè)委員會(huì)委員,福建省海峽腫瘤防治科技交流協(xié)會(huì)甲狀腺腫瘤分會(huì)委員,廈門市醫(yī)師協(xié)會(huì)病理醫(yī)師分會(huì)第一屆委員會(huì)委員,廈門醫(yī)師協(xié)會(huì)腫瘤青委胃腸學(xué)組成員。淋巴造血系統(tǒng)、泌尿系統(tǒng)、消化系統(tǒng)腫瘤等及炎癥性腸病病理診斷。