近日,,《歐洲核醫(yī)學與分子影像雜志》(Eur J Nucl Med Mol Imaging,Q1區(qū),,2021 IF=10.057)刊登了來自廈門大學附屬第一醫(yī)院核醫(yī)學科及腫瘤放療科團隊關于“68Ga-FAPI PET/CT預測食管癌根治性放化療預后”的臨床研究,。改研究通過PET/CT分子影像的方法為食管癌患者放化療的預后預測提供了新方法。論文通訊作者為核醫(yī)學科陳皓鋆教授,,放療科林勤教授,。

【研究背景】
食管鱗狀細胞癌 (ESCC) 是東亞地區(qū)食管癌的主要組織學亞型,而食管腺癌更常見于西歐和北美地區(qū),。中國患者的人數(shù)占全球 ESCC 患者的一半以上,。目前,食管癌根治性切除術是非轉(zhuǎn)移性ESCC的主要治療手段,。然而,,50%以上的ESCC患者就診時已是晚期,失去了手術機會,。對于不可切除和局部晚期的ESCC患者,,其治療主要依靠放射治療或放化療聯(lián)合的綜合治療,,但總體預后不良。針對這類患者,,準確判斷預后或總生存率的指標是非常必要的,,這將有利于及時優(yōu)化治療策略,提高生存率,。
諸多研究顯示臨床腫瘤分期(T分期)和區(qū)域淋巴結分期(N分期)可以預測各類非轉(zhuǎn)移性癌癥的臨床預后,。然而,僅僅通過臨床分期的結果可能并不足以預測 ESCC 患者的預后,。另有研究報告表明,,通過常規(guī)影像學技術監(jiān)測腫瘤治療前后形態(tài)大小的變化,可以早期評估ESCC 患者的治療響應,,預測預后,。例如,CT和磁共振成像(MRI)的圖像參數(shù)和紋理特征與接受放化療的患者的預后具有統(tǒng)計學顯著相關性,。[18F]FDG PET/CT是一種廣泛用于腫瘤檢測,、分期和治療反應評估的分子影像技術。在過去的十年里,,大量研究報告了[18F]FDG PET/CT代謝參數(shù)與多種惡性腫瘤臨床預后之間的關系,,在監(jiān)測治療療效、制定個體化治療方案中發(fā)揮重要的作用,。
隨著分子影像技術的不斷發(fā)展與成熟,,新近研究報告了一種靶向成纖維細胞活化蛋白 (FAP) 的新型放射性分子影像探針(FAPI)可應用于對多種實體瘤的PET/CT顯像。也有相關個案報告了FAPI PET/CT 對于ESCC 轉(zhuǎn)移淋巴結及骨/內(nèi)臟遠處轉(zhuǎn)移灶的檢出方面顯著優(yōu)于 [18F] FDG PET/CT,。此外,,我們及其他課題組的前期研究證明[68Ga]Ga-FAPI PET/CT 可為食管癌放射治療的靶區(qū)勾畫方案提供補充信息,。然而,,尚無[68Ga]Ga-FAPI PET/CT 預測惡行腫瘤預后價值的研究報告。在本研究中,,我們旨在分析[68Ga]Ga-FAPI PET/CT可否預測食管鱗癌根治性放化療的預后,,為食管癌患者的預后評估提供依據(jù)。
【研究方法】
回顧性分析本院2019-2020年期間接受根治性放化療且隨訪資料完整的ESCC患者37例,。根據(jù)實體瘤療效評估標準 (RECIST) 1.1 版評估臨床預后(無進展生存期 [PFS]和總生存期 [OS]),。本研究中位隨訪時間為 24 個月(范圍,16-29個月),。隨訪過程中有19 例ESCC患者出現(xiàn)疾病進展,,其中18例死于食管癌。
原發(fā)灶GTV測量方法:在原發(fā)灶放射性濃聚區(qū)域范圍內(nèi)以40%SUVmax為閾值,,工作站軟件自動勾畫感興趣區(qū)(Region of interest,,ROI),,并根據(jù)橫斷面、矢狀面,、冠狀面3個層面的圖像進行手工調(diào)節(jié),,盡量準確地使各層面原發(fā)灶均包含在ROI內(nèi),軟件自動計算得出GTVFAPI,,單位為cm3,。TL-FAPI = GTV x SUVmean。
采用IBM SPSS 22.0軟件進行統(tǒng)計分析,。計量資料正態(tài)分布通過K-S檢驗(以均數(shù)±標準差)表示,。連續(xù)變量如SUVmax、GTV,、TL-FAPI轉(zhuǎn)換為二分類變量進行統(tǒng)計分析,,利用ROC曲線尋找SUVmax、GTV,、TL-FAPI的最佳界值將其分為高值組及低值組,。生存分析采用Kaplan-Meier法進行單因素分析,組間生存曲線比較采用Log-rank檢驗,,P<0.05差異有統(tǒng)計學意義,。
【研究結果】
1. 不同TNM期間FAPI-PET的參數(shù)比較
FAPI-PET參數(shù)(SUVmax-FAPI: 最大標準攝取值; GTVFAPI: FAPI陽性腫瘤的大體體積; TL-FAPI: FAPI陽性總累積病灶,TL-FAPI = SUVmean × GTVFAPI)的定量分析結果顯示,,不同T分期患者間的FAPI-PET參數(shù)具有顯著統(tǒng)計學差異(圖1),。例如,T4期患者的多個FAPI-PET 參數(shù)顯著高于T2/T3期患者:SUVmax-FAPI (17.6 ± 5.7 vs. 13.3 ± 4.9, P = 0.009),、GTVFAPI (46.0 ± 34.7 cm3 vs. 14.7 ± 10.1 cm3,,P < 0.001)和 TL-FAPI(444.2 ± 315.7 g vs. 118.7 ± 92.1 g,P < 0.001),。然而,,不同N分期患者間的PET參數(shù)無統(tǒng)計學差異。
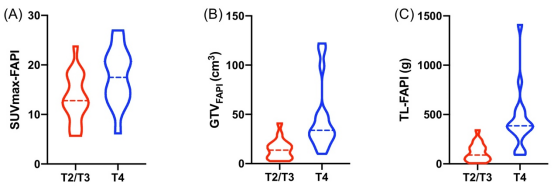
圖 1. T2/T3腫瘤與T4腫瘤間SUVmax-FAPI (A),、GTVFAPI (B)和TL-FAPI (C) 的差異,。
2. FAPI-PET參數(shù)與臨床預后之間的相關性分析
通過ROC曲線計算GTVFAPI和TL-FAPI 預測 PFS 的最佳cut-off值。GTVFAPI 和 TL-FAPI的最佳cut-off值分別為33.9 cm3(ROC 曲線下面積 [AUC] = 0.737,;P = 0.019)和226.7g(AUC = 0.726,;P = 0.025)(圖 2A-B)。隨后通過ROC曲線計算GTVFAPI和TL-FAPI預測OS的最佳cut-off值,,其最佳cut-off值與預測PFS值的cut-off值相同,。GTVFAPI和TL-FAPI 的 AUC 值均 > 0.75(圖 2C-D)。然而,根據(jù)SUVmax計算出的最佳cut-off值與PFS(SUVmax = 13.4,;AUC = 0.609,;P = 0.282)或OS(SUVmax = 18.2;AUC = 0.630,;P = 0.196)均無統(tǒng)計學關聯(lián),。
GTVFAPI ≤ 33.9 cm3 的ESCC患者較 GTVFAPI > 33.9 cm3 患者具有更好的 PFS(圖 3A,P = 0.005),。同樣,,以最佳TL-FAPI的cut-off值(226.7g)為界,兩組患者間的PFS存在統(tǒng)計學差異(P < 0.001,,圖 3B),。圖 3C-D顯示了GTVFAPI和TL-FAPI在OS預測中的Kaplan-Meier生存曲線。這些PET參數(shù)與患者的OS呈負相關,。例如,, GTVFAPI高值組(>33.9 cm3 , n=9)的1年生存率顯著高于GTVFAPI低值組(GTV≤33.9 cm3,n=25),,兩組的OS生存曲線具有統(tǒng)計學差異(80% vs. 22%,,P < 0.001)。具有代表性的baseline PET/CT和治療后follow-up CT圖像如圖4所示,。
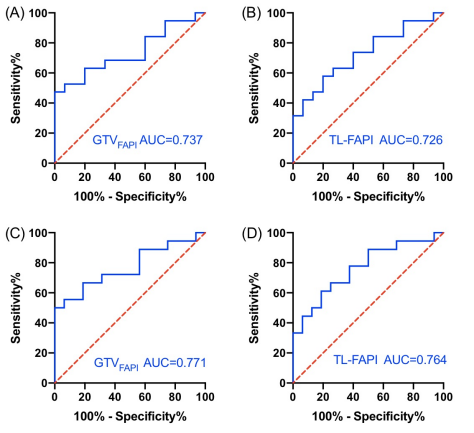
圖 2. 與無進展生存期(PFS)相關GTVFAPI (A) 和TL-FAPI (B)最佳界值的ROC曲線,。 與總生存期(OS)相關GTVFAPI (C) 和 TL-FAPI (D) 最佳界值的ROC曲線。
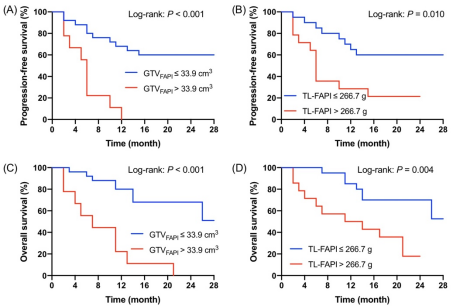
圖 3. 根據(jù)GTVFAPI (A) 和 TL-FAPI (B) 分組的無進展生存期(PFS)的 Kaplan-Meier 曲線,。 根據(jù)GTVFAPI (C) 和 TL-FAPI (D) 分組的總生存期(OS)的Kaplan-Meier 曲線,。
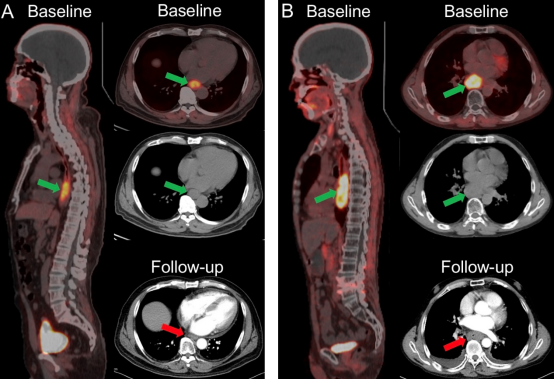
圖 4. (A) 男,62 歲,,ESCC初診患者,,接受PET/CT進行腫瘤分期。 [68Ga]Ga-FAPI PET/CT (GTVFAPI) 計算基線GTV為17.1 cm3 (<33.9 cm3),。隨訪增強 CT(治療后1個月)判定為部分緩解(PR),。該患者的總生存期為29個月(生存,隨訪中),。(B) 男,,52 歲,ESCC初診患者,,接受PET/CT進行腫瘤分期?;€GTV-FAPI為43.3 cm3 (>33.9 cm3),。隨訪增強CT判定為疾病穩(wěn)定(SD)。該患者的總生存期為11個月,。
3. 食管癌的單變量和多變量分析
單變量分析顯示,,PFS 與 T 分期,、N 分期、GTVFAPI 和 TL-FAPI 相關,,而 OS 與 T分 期,、GTVFAPI 和 TL-FAPI 相關,但與 N 分期無關(表 1),。在多變量分析中,,只有 GTVFAPI 是 PFS(HR,5.76,;95% CI,,2.13-15.57,P = 0.001)和 OS(HR,,4.96,;95% CI,2.55–18.79, P = 0.001)的獨立預后因素,。
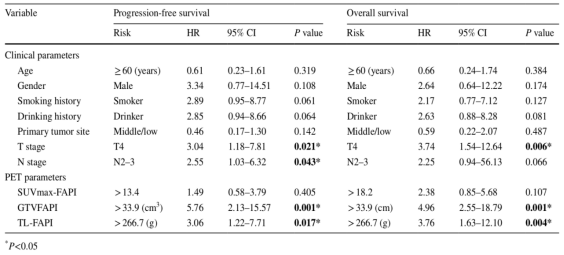
表1. 用于預測無進展生存期和總生存期 Cox 回歸模型的單變量分析
結論: 對于不可切除的晚期食管癌患者來說,,治療前基線[68Ga]Ga-FAPI PET/CT原發(fā)灶GTVFAPI、TL-FAPI對判斷其接受根治性放化療的預后具有一定預測價值,。高GTVFAPI,、高TL-FAPI的患者預后較差,GTVFAPI可用作接受根治性放化療ESCC 患者臨床PFS和OS的獨立預后因素,。因此,,治療前可根據(jù)這些參數(shù)對患者進行危險分層,從而制定個體化治療方案來改善預后,。未來尚需更大樣本和更長觀察期的進一步研究,。
原文地址:https://doi.org/10.1007/s00259-022-05989-1
作者風采
通訊作者 陳皓鋆

陳皓鋆,廈門大學附屬第一醫(yī)院核醫(yī)學科及閩南PET中心副主任醫(yī)師,,現(xiàn)任中國醫(yī)師協(xié)會核醫(yī)學分會青年委員,,中華醫(yī)學會核醫(yī)學分會淋巴瘤PET/CT工作委員會委員。榮獲福建省杰出青年基金資助,、全國青年崗位能手,、福建省衛(wèi)生健康中青年領軍人才、廈門市青年雙百人才,、中華醫(yī)學會核醫(yī)學分會“希望之星”獎,;曾獲北美核醫(yī)學會(SNMMI)最受矚目“青年科學家獎”(Ones to Watch, 全球30名)、SNMMI“臨床研究獎”第1名,;歐洲核醫(yī)學會(EANM)“年度最佳論文獎”,,亞洲分子影像學會(FASMI)“青年科學家”獎等多項國際重要獎項。主持國家自然科學基金項目2項、福建省中青年重大項目1項,;近5年以第一/通訊作者在醫(yī)學影像領域頂刊Radiology,、J Nucl Med、Eur J Nucl Med Mol Imaging發(fā)表研究論文25余篇,,以第一完成人獲廈門市科技進步獎1項,。
通訊作者 林勤

林勤,主任醫(yī)師,,廈門大學教授,,博士生導師,廈門大學附屬第一醫(yī)院黨委副書記?,F(xiàn)任中華醫(yī)學會放射腫瘤治療學分會委員,,福建省醫(yī)學會放射腫瘤治療學分會副主任委員,福建省抗癌協(xié)會鼻咽癌專業(yè)委員會副主任委員,,廈門市醫(yī)學會腫瘤放療分會主任委員,。任《中華放射醫(yī)學與防護雜志》等多種期刊編委。美國得克薩斯大學M.D. Anderson 癌癥中心訪問學者,,美國Duke University訪問學者,。主持或已主持國家自然科學基金、福建省衛(wèi)生廳,、廈門市科技局及全國多中心前瞻性臨床研究廈門分中心等多項課題,。研究內(nèi)容多次在美國國際放射腫瘤學年會上壁報交流。近五年以通訊作者在Eur J Nucl Med Mol Imaging,、Radiotherapy & Oncology,、Theranostics、中華核醫(yī)學與分子影像雜志等期刊發(fā)表研究論著20余篇,。主要研究方向:分子影像引導下的鼻咽癌,、肺癌、肝癌等領域的腫瘤精確放療以及SBRT(立體定向低分割放射治療),。
第一作者 趙亮

趙亮,,廈門大學附屬第一醫(yī)院腫瘤學博士研究生在讀,導師林勤教授和陳皓鋆副主任醫(yī)師,,研究方向為分子影像引導下腫瘤診療一體化,,第一作者(含共一)發(fā)表SCI論著15篇,中文核心論文1篇,。曾獲國家獎學金,、廈門大學本棟獎學金和唐立新獎學金。
共同一作 逄一臻

廈門大學2021級博士研究生,,中共黨員,,曾獲廈門大學醫(yī)學院“優(yōu)秀團員”,,廈門大學“三好學生”,、廈門大學“優(yōu)秀畢業(yè)生”,、廈門大學醫(yī)學院“遠思獎學金”、廈門大學“鷺燕獎學金”,、廈門大學校慶獎學金“本棟獎學金”,、研究生“國家獎學金”等榮譽。以第一或共同第一作者在Radiology,、Eur J Nucl Med Mol Imaging,、Clin Nucl Med等國際一流期刊發(fā)表多篇SCI期刊論文。
共同一作 陳珊宇

陳珊宇,,廈門大學附屬第一醫(yī)院腫瘤放射治療科副主任醫(yī)師,,畢業(yè)于華中科技大學同濟醫(yī)學院,2011年中山大學腫瘤防治中心進修腫瘤放療專業(yè),。畢業(yè)后至今一直從事腫瘤放射治療專業(yè)?,F(xiàn)任中國醫(yī)師協(xié)會放射腫瘤治療醫(yī)師分會食管癌放療組委員;福建省抗癌協(xié)會放射腫瘤專業(yè)委員會營養(yǎng)組委員,;福建省抗癌協(xié)會第一屆腫瘤科普專業(yè)委員會委員,;福建省醫(yī)學會放射腫瘤治療學分會第二屆委員會青年委員會委員;福建省醫(yī)學會放射治療學分會胸部放射治療學委員,。能嫻熟處理頭頸部,,胸部,腹部等各種惡性腫瘤,。已在專業(yè)期刊發(fā)表多篇專業(yè)論著,。